保健品之世界首款可注射大麻
"打针喝大麻"听起来像是科幻电影的桥段,但在创新无止境的美国市场,这已成为现实!
近日,加州一家名为Pico IV的初创公司因销售可静脉注射的大麻CBD产品而收到FDA(美国食品药品监督管理局)的严厉警告函,瞬间引爆了保健品膳食补充剂行业的热议。
"世界首款"引发监管地震
据了解,Pico IV公司自称提供"世界上第一款可注射CBD产品"。
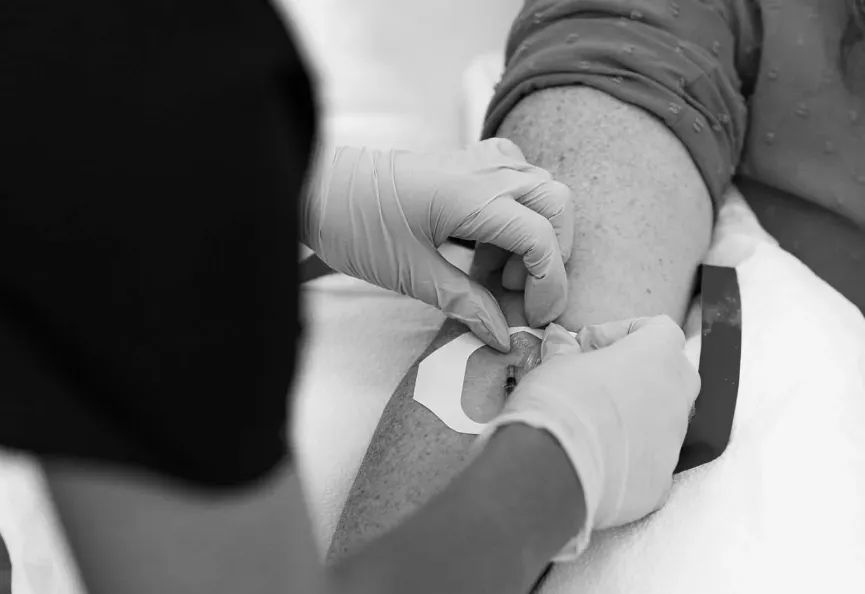
这款产品是一种纯化版CBD(大麻中的非致幻化合物),专为通过静脉输液注入血液而设计。

这家萨克拉门托的公司在其官网上打出了治疗慢性疼痛、克罗恩病和关节炎的旗号,并提供了多份"推荐信"作为佐证。
然而,FDA可不这么认为!在周一发出的警告信中,FDA明确指出Pico IV将这种注射产品作为"膳食补充剂"进行营销是违法的。
更严重的是,FDA特别强调这款产品"尤其令人担忧",因为直接向血液中注射任何物质都可能"导致严重且危及生命的疾病"。

来自美国FDA官网通告,原文较长,只截取了关键的内容
企业回应:安全是"首要任务"
面对FDA的警告,Pico IV首席执行官乔·杨(Joe Young)迅速做出回应。
他在发给SFGATE的电子邮件声明中表示:"公共安全是我们的首要任务",并强调公司产品经过了"旨在确保无菌和安全"的严格流程。
"我们对我们产品的安全性充满信心,并正在努力向FDA提供必要的信息,以解决他们的担忧。"
杨在声明中进一步解释道。
根据Pico IV官网信息,其产品由美国种植的大麻植物制成,属于某些大麻植物的合法类别,并宣称产品"完全无菌,静脉注射安全"。
值得注意的是,该公司网站还特别提到,这类产品不面向常规零售渠道,仅供"医生、服务提供商和静脉注射治疗诊所"购买。

专家担忧不无道理
毒理学专家们对此类产品的担忧并非空穴来风。
长期以来,大麻产品因不受严格的联邦安全标准约束而备受质疑。
更为关键的是,这类产品更容易受到重金属和杀虫剂的污染,这对于静脉注射产品而言无疑是致命隐患。
虽然Pico IV在官网上声称其所有产品均经过第三方实验室的纯度测试,但FDA的警告信似乎表明,这些测试可能并不足以满足注射类药品的严格安全标准。
给跨境保健品/膳食补充剂商家的启示
1.监管先行:在引进新产品前,务必全面了解目标市场的监管要求。
特别是涉及特殊剂型(如注射剂)时,审批流程通常更为严格。
2.市场定位要准:膳食补充剂≠药品。
将具有药物使用途径的产品标榜为膳食补充剂,是踩监管红线的危险行为。
3.产品宣称需谨慎:治疗功效宣称是FDA等监管机构的重点审查对象。
没有充分临床依据的功效宣称可能招致法律风险。
4.重视第三方验证:虽然第三方测试很重要,但需确保测试标准与产品预期用途相匹配。
注射类产品的安全标准远高于口服产品。
5.持续关注政策动态:大麻相关产品的监管环境在各国持续变化,密切跟踪政策动向是规避风险的关键。
无论创新多么前卫,消费者安全永远是底线。对于跨境保健品商家而言,合规经营、理性创新才是长久之道。
您对此有什么看法?欢迎在评论区分享您的观点!










